L'imballaggio primario è il primo strato che contiene direttamente un medicinale (o sigilla direttamente la dose). Può sembrare un dettaglio di confezionamento, ma spesso determina se un prodotto rimane stabile, sicuro e uniforme dalla produzione all'uso da parte del paziente.
Per molte compresse e capsule, anche una "piccola" modifica – come il passaggio dal blister al flacone, la sostituzione della lamina o l'utilizzo di un rivestimento diverso – può alterare l'esposizione all'umidità, il contatto con l'ossigeno o la protezione fisica. Per questo motivo, molti produttori considerano l'imballaggio primario non solo come un "contenitore", ma come un sistema di protezione che può influire sulla durata di conservazione, sul rischio di rottura e sull'affidabilità delle decisioni relative al rilascio dei lotti.
Un modo semplice per capirlo: se si rimuovesse tutto tranne lo strato che effettivamente contiene e protegge la dose, ciò che rimarrebbe sarebbe in genere l'imballaggio primario. Avere questa definizione chiara semplifica di molto il confronto tra formati, materiali e (più avanti in questo articolo) le tipiche attrezzature di confezionamento e il flusso di linea generale associati a ciascuna opzione.

Nozioni di base sull'imballaggio primario
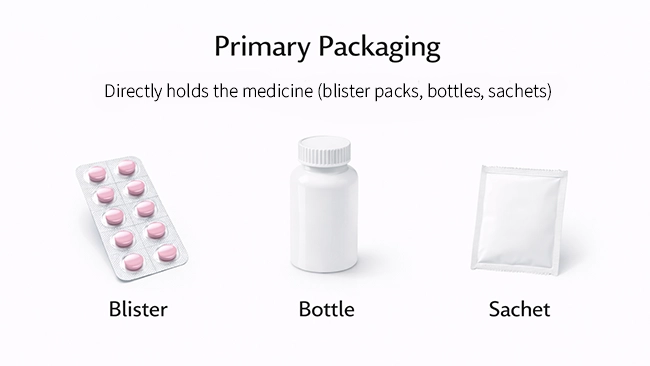
Si tratta della confezione che contiene direttamente il medicinale e costituisce la barriera immediata tra il prodotto e l'ambiente esterno. Nella maggior parte dei casi, è anche lo strato che crea il "sigillo" che protegge la dose.
Tra gli esempi più comuni si annoverano:
●
Confezioni blister
:
il blister formato che contiene ogni compressa/capsula più il materiale di chiusura (spesso un foglio di alluminio) che lo sigilla.
●
Bottiglie
: la bottiglia più il sistema di chiusura (tappo, guarnizione, sigillo a induzione ove applicabile). In altre parole, il "sistema bottiglia", non solo la forma della bottiglia.
●
Bustine/bustine
: la struttura del film che contiene e sigilla direttamente la polvere, i granuli o la singola dose.
●
Fiale/ampolle
: il contenitore stesso e, per le fiale, il tappo + la guarnizione come parte del sistema di chiusura.
●
siringhe preriempite
: il cilindro e i componenti di chiusura che mantengono il farmaco sigillato e protetto.
Ciò che di solito non viene considerato imballaggio primario:
●
Scatole di cartone, foglietti illustrativi, confezioni/pellicole termoretraibili e la maggior parte degli strati esterni di etichettatura. Si tratta in genere di imballaggi secondari o terziari, comunque importanti, ma non la prima barriera protettiva.
Imballaggio primario vs imballaggio secondario
Se l'imballaggio primario è quello che "protegge la dose", l'imballaggio secondario è spesso quello che "organizza e comunica la dose".
●
L'imballaggio primario si concentra sulla protezione: barriera contro umidità, ossigeno e luce, integrità della sigillatura, compatibilità e protezione fisica.
●
L'imballaggio secondario si concentra sulla presentazione e sulle informazioni: spazio per l'etichettatura, elementi di sicurezza antimanomissione, istruzioni per il paziente e organizzazione dell'unità (come astucci contenenti più blister o flaconi).
Un esempio pratico:
●
Il blister è un imballaggio primario perché ogni blister costituisce una barriera sigillata attorno alla dose.
●
La scatola che contiene il blister è solitamente un imballaggio secondario perché non sigilla direttamente la dose, ma contiene etichette, foglietti illustrativi e funge da supporto fisico durante la distribuzione.
Questa distinzione è importante perché quando cambia l'imballaggio, spesso si presta maggiore attenzione al rischio di stabilità e alle aspettative in termini di documentazione. Gli enti regolatori considerano il concetto di contenitore-chiusura come parte integrante della storia di qualità del prodotto, non solo come una scelta di marketing.
Food and Drug Administration degli Stati Uniti
)
Cosa protegge l'imballaggio primario: umidità, ossigeno, luce e manipolazione
Protezione dall'umidità
Molti prodotti in forma solida (inclusi i comuni integratori) sono sensibili all'umidità. L'umidità può alterare la durezza delle compresse, accelerarne la degradazione o causare l'ammorbidimento o l'adesione delle capsule. I formati primari come i blister ad alta barriera o i sistemi di flaconi ben progettati contribuiscono a rallentare l'esposizione all'umidità.
Protezione dell'ossigeno
L'ossigeno è un nemico lento e invisibile per alcuni principi attivi ed eccipienti. Un imballaggio "sufficientemente buono" per un prodotto potrebbe non esserlo per un altro con una maggiore sensibilità all'ossidazione. L'obiettivo non è la perfezione, ma ridurre l'esposizione all'ossigeno quel tanto che basta per raggiungere la durata di conservazione prevista.
Protezione dalla luce
La sensibilità alla luce è facile da sottovalutare perché il prodotto può apparire integro mentre il principio attivo si degrada lentamente. Flaconi ambrati, blister opachi e astucci possono tutti contribuire a questo fenomeno, ma la vera "prima barriera" rimane lo strato a contatto con la dose.
Protezione fisica e integrità della dose
Anche quando la composizione chimica è stabile, i danni fisici possono causare problemi di qualità: compresse rotte, polverizzazione, bordi scheggiati o capsule che perdono la loro finitura pulita. L'imballaggio primario contribuisce inoltre a mantenere l'integrità della dose durante la spedizione e la movimentazione, soprattutto per le compresse rivestite, le forme fragili e i prodotti con più referenze.
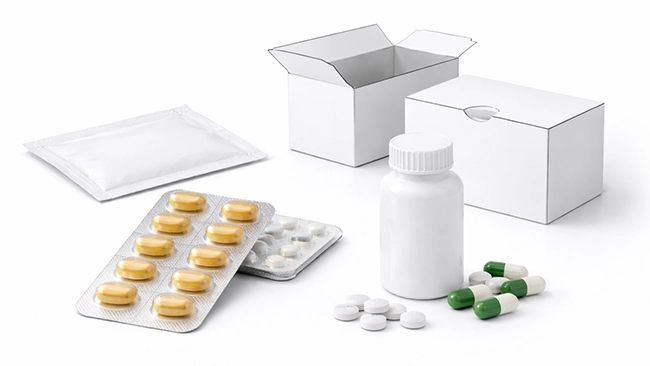
Formati di confezionamento primario per i medicinali
Ecco un semplice paragone che puoi utilizzare quando ragioni in termini di "formato prima di tutto" (e non di chimica dei materiali). È anche qui che "ciò che protegge" inizia a collegarsi naturalmente alle apparecchiature di confezionamento a valle.
|
Formato primario
|
medicinali comuni
|
Ciò che protegge meglio
|
Compromessi tipici
|
Implicazioni relative alle apparecchiature
|
|
Confezioni blister (monodose)
|
Compresse, capsule
|
Ottimo controllo dell'umidità/ossigeno (con il coperchio giusto); protezione dose per dose; forte indicatore di manomissione.
|
La scelta del design e dei materiali è importante; i cambi di formato richiedono attrezzature specifiche; lo spazio per la grafica sul lato del blister è limitato.
|
Spesso abbinato a una macchina per il confezionamento in blister, seguita dall'inscatolamento per il confezionamento secondario.
|
|
Bottiglie + sistema di chiusura
|
Compresse, capsule, caramelle gommose
|
Comodo per i consumatori; formati di conteggio flessibili; più spazio per l'etichettatura
|
Il controllo dell'umidità/ossigeno dipende in larga misura dal sistema di chiusura/rivestimento e dallo spazio di testa; l'abrasione delle compresse può rappresentare un problema.
|
Spesso abbinato a una linea di conteggio e imbottigliamento (conteggio/riempimento + tappatura), con possibilità di inscatolamento.
|
|
Bustine / bustine monodose
|
Polveri, granuli, alcuni effervescenti
|
Buona protezione monodose; portabilità; controllo delle porzioni
|
La qualità della sigillatura e la scelta della pellicola sono importanti; meno pratico per le procedure multidose.
|
Spesso si abbina a
macchina per confezionamento in stick
/ macchina confezionatrice per bustine; astuccio opzionale a seconda della presentazione
|
|
Fiale/ampolle
|
Liquidi, iniettabili
|
Robusta protezione del contenitore
|
Il formato è meno flessibile; spesso comporta una maggiore complessità di imballaggio e gestione.
|
Tipicamente associato ai sistemi di riempimento e confezionamento sterili (che esulano dall'ambito di questo articolo).
|
|
siringhe preriempite
|
Farmaci biologici, iniettabili
|
Comodità di dosaggio; manipolazione ridotta
|
Elevate aspettative in termini di qualità dei componenti.
|
Sistemi sterili specializzati; non paragonabili alle linee per dosi solide.
|
Se i tuoi prodotti sono principalmente compresse/capsule, blister e flaconi sono solitamente oggetto della maggior parte delle decisioni pratiche.
Materiali: plastica, fogli di alluminio, vetro
Spesso la scelta dei materiali può risultare complicata, quindi è importante mantenere l'obiettivo semplice: i materiali determinano il comportamento della barriera e il rischio di compatibilità.
●
Le materie plastiche (utilizzate per bottiglie, alcune pellicole per blister e buste) presentano un'ampia varietà di proprietà di barriera all'umidità e all'ossigeno. "Plastica" non è un unico tipo, ma una famiglia di materiali.
●
Le lamine e le pellicole multistrato (soprattutto in blister e bustine) possono fornire barriere molto più resistenti rispetto a molte materie plastiche, ma comportano dei compromessi in termini di costi, riciclabilità e possibilità di formatura/sigillatura.
●
Il vetro (comunemente utilizzato in fiale e alcune bottiglie) è spesso considerato un materiale con un'elevata capacità di barriera, ma la protezione complessiva dipende comunque dall'intero sistema di chiusura del contenitore, non dal contenitore stesso.
Un utile principio da principiante: il formato determina il risultato, i materiali determinano la qualità del risultato. Per questo motivo, formato primario e materiale vengono spesso discussi insieme nella pianificazione della stabilità, soprattutto per i prodotti destinati a una maggiore durata di conservazione o a condizioni di distribuzione più difficili.
Sistema di chiusura del contenitore
Gli enti regolatori e i produttori esperti parlano spesso di un sistema di chiusura per contenitori perché la vera protezione deriva dall'intero sistema, non da un singolo componente. Ad esempio, una bottiglia priva di un rivestimento interno o di una strategia di sigillatura adeguati può comportarsi in modo molto diverso rispetto alla stessa bottiglia dotata di un sistema di chiusura migliore.
Concetti chiave:
●
Sistema di chiusura dei contenitori (CCS)
: il contenitore + tutti i componenti che creano e mantengono la chiusura (tappo, rivestimento interno, sigillo in alluminio, tappo di chiusura, ecc.).
●
Integrità del sigillo
La tenuta della guarnizione rimane affidabile nel tempo e nelle condizioni di spedizione/movimentazione previste?
●
Compatibilità
: Il prodotto e i componenti dell'imballaggio possono interagire in modi che ne influenzano la qualità (ad esempio, adsorbimento, migrazione o trasferimento di odori)?
●
Cambiare spettro
Le modifiche al packaging possono innescare una rivalutazione, poiché piccole differenze nei componenti possono alterare le ipotesi relative alle prestazioni o ai rischi.
Come l'imballaggio primario si collega alle attrezzature di confezionamento e al flusso di processo
Passaggio 1: Iniziare dalla forma farmaceutica
La maggior parte dei farmaci orali solidi inizia il proprio ciclo di vita sotto forma di compresse o capsule riempite. Questa scelta iniziale solitamente implica l'utilizzo di macchinari come una comprimitrice o una macchina riempitrice di capsule nelle fasi precedenti del processo, ma questo articolo si concentra su ciò che accade quando il prodotto è pronto per essere confezionato.
Fase 2: La scelta definisce il “percorso di confezionamento”
Una volta che la dose è pronta, la decisione sul confezionamento tende a definire un flusso di confezionamento tipico:
●
Flusso a blister (a dose unitaria):
Le dosi vengono disposte e sigillate in cavità blister, quindi trasferite in imballaggi secondari come i cartoni. In termini di attrezzature, di solito vedrai un
macchina per il confezionamento in blister
seguito da un
macchina per l'incarto
(e talvolta fasi di stampa/ispezione a seconda del prodotto e delle esigenze del mercato).
●
Flusso con la bottiglia prima
: le dosi vengono contate (o altrimenti porzionate) in flaconi, quindi chiusi ed etichettati, con inscatolamento opzionale per la presentazione al dettaglio o per una maggiore protezione. In termini di attrezzature, questo comporta comunemente un
macchina conta-compresse
(o una linea di conteggio e imbottigliamento più ampia) e poi operazioni a valle come la tappatura e l'inscatolamento opzionale.
Passo 3: Perché è importante (anche in una guida per principianti)
Questo collegamento ti aiuta a evitare due errori comuni:
1. decidere un formato primario senza considerare se la linea può mantenere una produzione e una protezione costanti e
2. Presumere che una modifica dell'imballaggio sia "solo una modifica dell'imballaggio" quando potrebbe alterare il rischio di stabilità e le aspettative in termini di documentazione.
Errori comuni dei principianti
Errore 1: "Una barriera più robusta è sempre meglio."
A volte sì, ma non sempre. Una barriera più alta può aumentare i costi, limitare la flessibilità del formato o creare compromessi con gli obiettivi di sostenibilità. La barriera "migliore" è quella che supporta in modo affidabile la durata di conservazione e le condizioni di utilizzo.
Errore 2: "L'imballaggio primario è separato dalla stabilità."
In pratica, la pianificazione della stabilità spesso considera l'imballaggio come parte integrante del modello di protezione del prodotto. La chiusura del contenitore e le condizioni di conservazione sono direttamente correlate alla durata di conservazione.
Errore 3: "Passare dal blister al flacone è una semplice decisione di marketing."
Può trattarsi di una decisione di branding, ma è anche un cambiamento del sistema di protezione: diverse modalità di esposizione all'umidità, diverse modalità di manipolazione fisica e diverse aspettative in termini di prove.
Errore 4: "Se si sigilla oggi, si sigilla per tutta la durata di conservazione."
L'affidabilità delle guarnizioni si basa sulle prestazioni nel tempo e sulla distribuzione delle sollecitazioni, non solo su un singolo momento della produzione.
Tendenze che influenzano le decisioni relative al packaging
Alcuni trend continuano a ripresentarsi sia nel settore farmaceutico che in quello degli integratori:
●
Pressione per la sostenibilità: maggiore interesse per le strutture riciclabili e la riduzione dei materiali, il che può creare nuovi compromessi che rappresentano un ostacolo.
●
Maggiori informazioni sulla confezione: tracciabilità, istruzioni più chiare e requisiti di etichettatura specifici per il mercato possono modificare le modalità di utilizzo degli imballaggi secondari, anche quando l'imballaggio primario rimane invariato.
●
Aspettative più elevate in termini di uniformità: con l'aumento del numero di referenze, i produttori si preoccupano maggiormente di garantire prestazioni di imballaggio prevedibili e scalabili.
Queste tendenze non individuano un unico formato "vincente", ma spingono gli acquirenti a porsi domande più precise su ciò che l'imballaggio deve effettivamente realizzare.
Un semplice schema per scegliere l'imballaggio primario
Se non hai familiarità con le decisioni relative al packaging, queste domande rappresentano un ottimo punto di partenza:
1. Quanto è sensibile il prodotto all'umidità, all'ossigeno o alla luce?
2. Quanto è fragile la dose durante la spedizione e la manipolazione quotidiana?
3. Come lo utilizzerà il cliente: per la praticità di una singola dose o per la comodità di dosi multiple?
4. Quali requisiti richiede il vostro mercato di riferimento in termini di etichettatura, sigilli di garanzia contro le manomissioni o protezione a prova di bambino?
5. Quale flusso di confezionamento si adatta al tuo piano di espansione: blister prima o flacone prima?
Se riuscite a rispondere a queste domande in modo chiaro, di solito eviterete gli errori di imballaggio più costosi.
Conclusione
L'imballaggio primario è il primo strato protettivo che avvolge il medicinale e, per molti prodotti, funge da parte integrante del prodotto stesso. Una volta compreso cosa si intende per imballaggio primario, è possibile confrontare formati e materiali con un obiettivo più chiaro: proteggere la stabilità, mantenere l'integrità della dose e garantire un uso sicuro.
Altrettanto importante è la scelta del formato primario, che si collega naturalmente al tipico flusso di confezionamento e alle macchine che lo gestiscono. Gli approcci che privilegiano il blister e quelli che privilegiano la bottiglia risolvono entrambi problemi diversi in modo efficace, e la scelta "giusta" è quella che meglio si adatta ai rischi del prodotto, al caso d'uso e alle esigenze di scalabilità.
FAQ
1) In che modo l'imballaggio primario influisce sulla durata di conservazione?
Controlla l'esposizione all'umidità, all'ossigeno e alla luce e protegge fisicamente la dose. Diversi formati/materiali possono modificare il profilo di rischio di stabilità del prodotto.
2) Che cos'è, in parole semplici, un sistema di chiusura per contenitori?
Si tratta del contenitore più tutte le parti che creano e mantengono la chiusura ermetica (tappo, rivestimento interno, sigillo in alluminio, tappo di chiusura, ecc.).
3) Cosa si intende per integrità del sigillo e perché è importante?
L'integrità della sigillatura si riferisce alla sua affidabilità durante lo stoccaggio e la distribuzione. Una sigillatura debole può compromettere la funzione di barriera da cui dipende il vostro prodotto.
4) Come si sceglie tra blister e flacone per compresse o capsule?
Iniziate considerando la sensibilità all'umidità e le esigenze di protezione della dose, quindi valutate la praticità d'uso e i requisiti di etichettatura. I blister spesso offrono una protezione ottimale della dose unitaria, mentre i flaconi sono spesso più pratici.
Riferimenti
FDA — Sistemi di chiusura dei contenitori per il confezionamento di farmaci e prodotti biologici per uso umano (linee guida).
































 Rete IPv6 supportata
Rete IPv6 supportata